Dinamika Enzimatis dan Regulasi Glikolisis Mikroba: Tinjauan Molekuler Jalur Embden-Meyerhof-Parnas
Dalam studi fisiologi mikroba tingkat lanjut, jalur Embden-Meyerhof-Parnas (EMP) tidak lagi dipandang sekadar sebagai urutan sepuluh reaksi linear konversi glukosa menjadi piruvat. Jalur ini merupakan pusat distribusi fluks karbon (carbon flux hub) yang sangat terintegrasi, yang diatur secara ketat oleh termodinamika dan jaringan regulasi genetik. Bagi mikroorganisme, efisiensi glikolisis ditentukan oleh adaptasi struktural enzim-enzim kuncinya terhadap lingkungan—baik itu ketersediaan energi, keberadaan oksigen, atau tipe substrat.
Table Of Content
- Plastisitas Tahap Fosforilasi: Pemanfaatan Donor Fosfat Alternatif
- Fosfofruktokinase (PFK): ATP-dependent vs PPi-dependent
- Mekanisme Katalitik Aldolase: Divergensi Evolusioner
- Kelas I vs Kelas II Aldolase
- Kopling Energi pada GAPDH: Peran Kritis Residu Sistein
- Regulasi Transkripsional: Di Luar Kontrol Alosterik
- Kesimpulan
- Daftar Pustaka
- Terkait
Analisis ini akan membedah kompleksitas enzimologi glikolisis, dengan fokus pada variasi filogenetik enzim kunci, mekanisme katalitik yang membedakan bakteri dari eukariota, serta strategi konservasi energi alternatif yang sering luput dari pembahasan dasar.

Plastisitas Tahap Fosforilasi: Pemanfaatan Donor Fosfat Alternatif
Dogma umum menyatakan bahwa fosforilasi glukosa dan fruktosa-6-fosfat (F6P) selalu bergantung pada ATP. Namun, pada tataran mikrobiologi molekuler, realitasnya jauh lebih beragam. Banyak mikroorganisme, terutama anaerob obligat dan beberapa Archaea, telah berevolusi untuk menggunakan donor fosfat yang lebih efisien secara termodinamika.
Fosfofruktokinase (PFK): ATP-dependent vs PPi-dependent
Enzim PFK adalah titik kontrol alosterik utama (rate-limiting step). Pada kebanyakan bakteri aerob (seperti E. coli) dan eukariota, PFK adalah ATP-dependent. Reaksi ini bersifat irreversible karena tingginya energi bebas yang dilepaskan. Namun, pada protista tertentu (seperti Entamoeba histolytica) dan bakteri (seperti Propionibacterium freudenreichii), ditemukan enzim PPi-PFK (Pirofosfat-fruktosa-6-fosfat kinase).
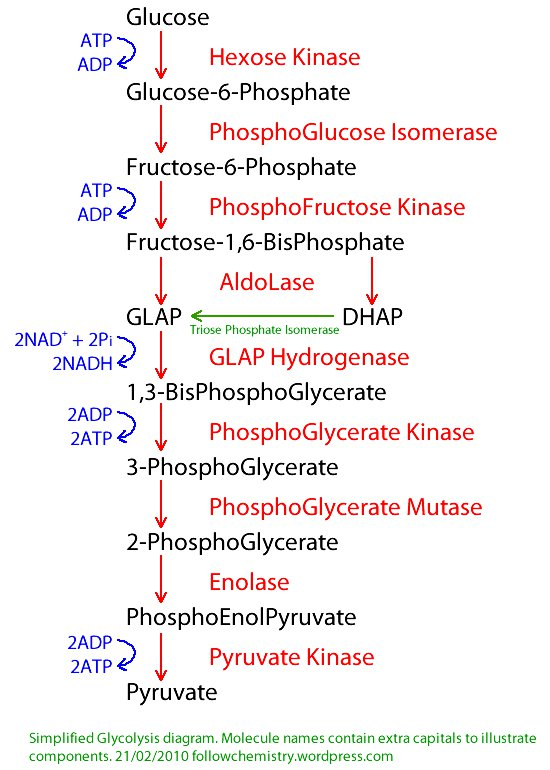
Signifikansi Bioenergetika: Penggunaan Pirofosfat (PPi) sebagai donor fosfat, alih-alih ATP, memberikan keuntungan energetik yang masif. PPi adalah produk sampingan biosintesis yang biasanya dihidrolisis. Dengan menggunakan PPi, mikroba ini menghemat ATP, sehingga hasil bersih ATP per glukosa bisa meningkat dari 2 menjadi 3 atau bahkan lebih. Reaksi PPi-PFK juga bersifat reversible, memberikan fleksibilitas metabolik yang lebih tinggi untuk glukoneogenesis tanpa memerlukan enzim bypass Fructose-1,6-bisphosphatase (Siebers & Schonheit, 2005).
Mekanisme Katalitik Aldolase: Divergensi Evolusioner
Pemecahan Fruktosa-1,6-bifosfat (FBP) menjadi triosa fosfat dikatalisis oleh enzim FBP Aldolase. Secara mekanistik dan filogenetik, enzim ini terbagi menjadi dua kelas yang sangat berbeda, yang menjadi target penting dalam pengembangan antimikroba selektif.
Kelas I vs Kelas II Aldolase
- Aldolase Kelas I: Umum ditemukan pada eukariota tingkat tinggi (termasuk manusia) dan beberapa bakteri. Mekanisme katalitiknya melibatkan pembentukan intermediet basa Schiff antara substrat dengan residu lisin pada sisi aktif enzim.
- Aldolase Kelas II: Ditemukan dominan pada bakteri dan fungi. Enzim ini adalah metaloenzim yang bergantung pada ion logam divalen (biasanya Zn2+ atau Fe2+) untuk menstabilkan intermediet enolat carbanion selama reaksi pemecahan C-C.
Karena manusia tidak memiliki Aldolase Kelas II, inhibitor spesifik yang menargetkan sisi pengikatan logam pada enzim bakteri ini menjadi kandidat potensial untuk antibiotik baru yang minim efek samping toksisitas pada inang (Pewsey et al., 2018).
Kopling Energi pada GAPDH: Peran Kritis Residu Sistein
Tahap oksidasi Gliseraldehida-3-fosfat (G3P) oleh enzim GAPDH adalah inti dari konservasi energi glikolisis. Di sini, energi oksidasi (eksergonik) “disimpan” dalam bentuk ikatan asil-fosfat berenergi tinggi (1,3-BPG).
Mekanisme Katalitik: Kunci reaksi ini terletak pada residu sistein di sisi aktif enzim yang memiliki gugus tiol (-SH) reaktif. Sistein ini menyerang gugus aldehida pada G3P, membentuk intermediet tiohemiasetal. Oksidasi oleh NAD+ kemudian mengubahnya menjadi ikatan tioester yang berenergi tinggi. Serangan selanjutnya oleh fosfat anorganik memecah ikatan tioester ini, menghasilkan 1,3-BPG. Jika residu sistein ini teroksidasi atau dihambat (misalnya oleh stres oksidatif atau logam berat), glikolisis akan terhenti total (Nelson & Cox, 2017).
Regulasi Transkripsional: Di Luar Kontrol Alosterik
Sementara buku teks dasar berfokus pada aktivasi/inhibisi alosterik (seperti ATP atau sitrat menghambat PFK), regulasi pada tingkat mikroba melibatkan kontrol transkripsional global yang merespons ketersediaan sumber karbon. Fenomena ini dikenal sebagai Carbon Catabolite Repression (CCR).
- Pada Bakteri Gram-Negatif (seperti E. coli): Sistem ini dimediasi oleh protein Cra (Catabolite Repressor/Activator). Cra berfungsi sebagai sensor fluks glikolitik. Ketika konsentrasi FBP rendah (menandakan glukosa langka), Cra berikatan dengan DNA dan mengaktifkan gen-gen untuk glukoneogenesis serta respirasi, sambil menekan gen glikolisis.
- Pada Bakteri Gram-Positif (seperti B. subtilis): Mekanismenya berbeda, menggunakan protein regulator CcpA (Carbon Catabolite Protein A). Kompleks CcpA-HPr(Ser-P) akan berikatan pada situs cre di DNA, menekan ekspresi gen-gen yang terlibat dalam pemanfaatan sumber karbon sekunder selama glukosa masih tersedia (Görke & Stülke, 2008).
Kesimpulan
Glikolisis pada mikroba bukanlah jalur statis yang seragam. Ia menunjukkan keragaman evolusioner yang luar biasa dalam hal pemilihan kofaktor enzim (Kelas I vs II Aldolase), strategi konservasi energi (ATP vs PPi), dan mekanisme regulasi genetik (Cra vs CcpA). Pemahaman mendalam mengenai variasi molekuler ini sangat esensial, tidak hanya untuk memetakan filogeni metabolisme, tetapi juga sebagai dasar rekayasa metabolik (metabolic engineering) dan penemuan target obat antimikroba baru.
Daftar Pustaka
- Görke, B., & Stülke, J. (2008). Carbon catabolite repression in bacteria: many ways to make the most out of nutrients. Nature Reviews Microbiology, 6(8), 613-624.
- Nelson, D. L., & Cox, M. M. (2017). Lehninger Principles of Biochemistry. 7th Edition. W.H. Freeman.
- Pewsey, E., et al. (2018). Class II fructose-1, 6-bisphosphate aldolase as a target for novel antimicrobial agents. FEMS microbiology letters, 365(10).
- Siebers, B., & Schönheit, P. (2005). Unusual pathways and enzymes of central carbohydrate metabolism in Archaea. Current opinion in microbiology, 8(6), 695-705.

