Enzim Glikolisis: Master Metabolisme dan Peran Ganda dalam Patologi Seluler
Selama puluhan tahun, buku teks biokimia mendefinisikan enzim glikolisis sebagai katalis “pekerja keras” yang tugasnya hanya satu: memecah glukosa menjadi piruvat untuk menghasilkan ATP. Pandangan ini, meskipun akurat secara metabolik, ternyata terlalu menyederhanakan realitas biologis yang jauh lebih kompleks. Riset proteomik modern mengungkapkan bahwa enzim-enzim purba ini menjalani kehidupan ganda atau moonlighting functions.
Table Of Content
- 10 Enzim Kunci Glikolisis: Tinjauan Struktural dan Fungsional
- Mekanisme Regulasi: Kontrol Flux yang Berlapis
- Kontrol Alosterik: Logika Energi Seluler
- Regulasi Hormonal: Peran Fruktosa-2,6-Bifosfat
- Fenomena Moonlighting: Ketika Enzim “Menyeleweng” dari Jalurnya
- Translokasi Nuklear: GAPDH dan Sinyal Kematian
- Penjaga Mitokondria: Heksokinase 2 (HK2)
- Signifikansi Klinis: Glikolisis dalam Penyakit
- Efek Warburg dan Peralihan Isoform PKM2
- Defisiensi Piruvat Kinase: Anemia Hemolitik
- Target Terapi Masa Depan
- Kesimpulan
- Daftar Pustaka
- Terkait

Di luar peran kanoniknya dalam sitoplasma, enzim glikolisis ditemukan bekerja di nukleus untuk mengatur ekspresi gen, menempel pada mitokondria untuk mencegah kematian sel, hingga berinteraksi dengan sitoskeleton untuk mempertahankan struktur sel. Bagi mahasiswa pascasarjana biosains, memahami enzim glikolisis kini berarti memahami dua dimensi sekaligus: peran sentralnya dalam bioenergetika (Metabolisme) dan peran non-kanoniknya dalam regulasi seluler (Signal Transduksi). Artikel ini akan membedah kedua dimensi tersebut, mulai dari kinetika enzim, mekanisme regulasi, hingga implikasi klinisnya dalam onkologi dan kelainan genetik.
10 Enzim Kunci Glikolisis: Tinjauan Struktural dan Fungsional
Jalur glikolisis terdiri dari sepuluh reaksi enzimatik yang terbagi menjadi dua fase utama: fase investasi energi dan fase pembayaran (payoff). Berikut adalah pemetaan enzim beserta peran spesifik dan fungsi tambahannya:
| Fase | Enzim | Reaksi Katalitik Utama | Fungsi “Moonlighting” / Fakta Unik |
|---|---|---|---|
| Investasi | 1. Heksokinase (HK) | Fosforilasi Glukosa → G6P (Irreversibel) | Isoform HK2 berikatan dengan VDAC di mitokondria, mencegah apoptosis pada sel kanker. |
| 2. Fosfoglukosa Isomerase (PGI) | Isomerisasi G6P → F6P | Di luar sel, dikenal sebagai Autocrine Motility Factor (AMF) yang memicu metastasis tumor. | |
| 3. Fosfofruktokinase-1 (PFK-1) | Fosforilasi F6P → F1,6-BP (Irreversibel) | Titik kontrol utama (rate-limiting step). Sangat sensitif terhadap rasio ATP/AMP. | |
| 4. Aldolase | Pemecahan F1,6-BP → DHAP + G3P | Berikatan dengan F-aktin, mengatur struktur sitoskeleton dan motilitas sel. | |
| 5. Triosa Fosfat Isomerase (TPI) | Interkonversi DHAP ↔ G3P | Enzim “sempurna” secara kinetik; laju reaksinya hanya dibatasi oleh difusi substrat. | |
| Payoff | 6. GAPDH | Oksidasi G3P → 1,3-BPG | Masuk ke nukleus saat stres oksidatif untuk memicu fragmentasi DNA dan kematian sel. |
| 7. Fosfogliserat Kinase (PGK) | Transfer fosfat 1,3-BPG → 3-PG (Hasilkan ATP) | Dapat bertranslokasi ke nukleus untuk memodulasi replikasi DNA virus. | |
| 8. Fosfogliserat Mutase (PGM) | Isomerisasi 3-PG → 2-PG | Memerlukan kofaktor 2,3-BPG pada banyak jaringan mamalia. | |
| 9. Enolase | Dehidrasi 2-PG → PEP | Pada permukaan sel (sebagai α-enolase), berfungsi sebagai reseptor plasminogen. | |
| 10. Piruvat Kinase (PK) | Transfer fosfat PEP → Piruvat (Irreversibel) | Isoform PKM2 bertindak sebagai ko-aktivator transkripsi gen di nukleus sel kanker. |
Mekanisme Regulasi: Kontrol Flux yang Berlapis
Sel harus menyeimbangkan produksi ATP dengan penyediaan prekursor biosintesis. Oleh karena itu, aktivitas enzim glikolisis diatur secara ketat melalui mekanisme alosterik dan hormonal.
Kontrol Alosterik: Logika Energi Seluler
Enzim PFK-1 bertindak sebagai sensor utama status energi sel. Aktivitasnya diatur oleh rasio ATP/AMP:
- Inhibisi oleh ATP: Saat energi melimpah (ATP tinggi), ATP berikatan dengan situs alosterik PFK-1, menurunkan afinitas enzim terhadap substrat Fruktosa-6-fosfat. Ini mencegah konsumsi glukosa yang tidak perlu.
- Aktivasi oleh AMP: Saat energi menipis, akumulasi AMP menggeser konformasi PFK-1 kembali ke bentuk aktif, memacu glikolisis untuk segera memproduksi ATP.
- Umpan Balik Sitrat: Sitrat, intermediat Siklus Krebs, juga menghambat PFK-1. Akumulasi sitrat menandakan bahwa kebutuhan biosintesis dan energi di hilir sudah terpenuhi, sehingga glikolisis harus diperlambat.
Regulasi Hormonal: Peran Fruktosa-2,6-Bifosfat
Regulasi jangka panjang, terutama di hati, dimediasi oleh hormon insulin dan glukagon yang mengontrol konsentrasi Fruktosa-2,6-Bifosfat (F-2,6-BP). Molekul ini adalah aktivator alosterik paling kuat bagi PFK-1.
Insulin memicu sintesis F-2,6-BP, yang kemudian mengaktifkan PFK-1 secara maksimal, mendorong glikolisis untuk menurunkan gula darah. Sebaliknya, glukagon menurunkan kadar F-2,6-BP, menghambat glikolisis dan mendorong glukoneogenesis. Mekanisme ini memastikan hati tidak “membakar” glukosa saat tubuh sedang membutuhkannya (puasa).
Fenomena Moonlighting: Ketika Enzim “Menyeleweng” dari Jalurnya
Aspek paling revolusioner dalam biokimia modern adalah pemahaman bahwa enzim glikolisis memiliki fungsi ganda yang krusial di luar metabolisme energi.
Translokasi Nuklear: GAPDH dan Sinyal Kematian
GAPDH secara klasik dikenal sebagai enzim dehidrogenase. Namun, di bawah kondisi stres oksidatif, residu sistein pada sisi aktif GAPDH mengalami modifikasi pascatranslasi berupa S-nitrosilasi (penambahan gugus NO). Modifikasi ini memungkinkan GAPDH berikatan dengan protein Siah1 dan masuk ke dalam nukleus. Di sana, kompleks ini bertindak sebagai “sirene kematian,” mengaktifkan p300/CBP dan memicu fragmentasi DNA yang berujung pada apoptosis (kematian sel terprogram). Ini menjelaskan mengapa agregasi GAPDH sering ditemukan pada penyakit neurodegeneratif seperti Alzheimer dan Parkinson.
Penjaga Mitokondria: Heksokinase 2 (HK2)
Pada sel kanker, isoform Heksokinase 2 (HK2) sering ditemukan menempel pada membran luar mitokondria, berikatan dengan kanal VDAC (Voltage-Dependent Anion Channel). Interaksi ini memiliki dua keuntungan strategis bagi kanker:
- Akses Prioritas ATP: HK2 mendapatkan akses langsung ke ATP yang baru diproduksi mitokondria, mempercepat laju glikolisis hingga 200 kali lipat.
- Efek Anti-Apoptosis: Ikatan HK2 memblokir pelepasan sitokrom c dari mitokondria, sehingga sel kanker menjadi kebal terhadap sinyal kematian sel.
Signifikansi Klinis: Glikolisis dalam Penyakit
Efek Warburg dan Peralihan Isoform PKM2
Sel kanker menunjukkan perilaku metabolik unik yang disebut Efek Warburg: mereka lebih memilih glikolisis aerobik (fermentasi laktat meski ada oksigen) daripada respirasi oksidatif. Kunci molekuler dari fenomena ini adalah peralihan isoform enzim Piruvat Kinase, dari PKM1 (tipe dewasa/otot) ke PKM2 (tipe embrionik).
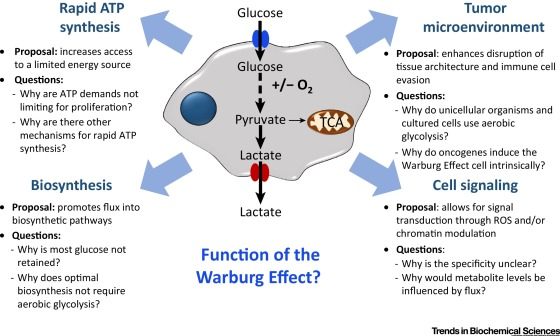
PKM2 cenderung berada dalam bentuk dimer yang kurang aktif secara katalitik. Akibatnya, konversi PEP menjadi piruvat melambat, menyebabkan penumpukan intermediat glikolisis di hulu. Penumpukan ini kemudian dialihkan ke jalur biosintesis (jalur Pentosa Fosfat) untuk memproduksi nukleotida, asam amino, dan lipid yang dibutuhkan untuk pembelahan sel yang cepat. Selain itu, dimer PKM2 dapat masuk ke nukleus dan bertindak sebagai ko-aktivator transkripsi untuk gen Oct4, yang menjaga sifat stemness sel kanker.
Defisiensi Piruvat Kinase: Anemia Hemolitik
Eritrosit (sel darah merah) tidak memiliki mitokondria dan bergantung 100% pada glikolisis untuk ATP. Mutasi pada gen PKLR menyebabkan enzim Piruvat Kinase menjadi tidak stabil atau kurang aktif. Akibatnya, produksi ATP di sel darah merah anjlok. Tanpa ATP yang cukup, pompa ion Na+/K+ gagal bekerja, keseimbangan osmotik terganggu, dan sel darah merah pecah (lisis) sebelum waktunya. Inilah patofisiologi dasar dari anemia hemolitik non-sferositik.
Target Terapi Masa Depan
Pemahaman mendalam tentang enzim glikolisis telah membuka jalan bagi kelas obat baru. Obat Mitapivat, yang baru disetujui FDA, bekerja sebagai aktivator alosterik yang menstabilkan tetramer enzim Piruvat Kinase pada pasien defisiensi PK, secara efektif “memperbaiki” enzim yang rusak tersebut.
Di bidang onkologi, strategi mengganggu interaksi “moonlighting” menjadi fokus utama. Molekul kecil seperti 3-Bromopyruvate (3-BrPA) dan inhibitor HK2-VDAC sedang dikembangkan untuk secara selektif membunuh sel kanker dengan cara memutuskan suplai energi mereka dan memicu kembali apoptosis, tanpa merusak sel normal yang menggunakan isoform enzim berbeda.
Kesimpulan
Enzim glikolisis bukanlah entitas statis dalam buku teks. Mereka adalah protein dinamis dengan plastisitas fungsional yang luar biasa—bertindak sebagai mesin energi, regulator genetik, hingga sensor kematian sel. Evolusi telah mengonservasi struktur mereka selama miliaran tahun, namun juga memodifikasinya untuk menjalankan fungsi ganda yang canggih. Bagi peneliti biomedis masa depan, tantangannya bukan lagi sekadar memetakan jalur metabolisme, melainkan memanipulasi fungsi ganda enzim-enzim ini untuk terapi penyakit kompleks mulai dari kanker hingga neurodegenerasi.
Daftar Pustaka
- Berg, J. M., Tymoczko, J. L., & Stryer, L. (2012). Biochemistry. 7th Edition. W.H. Freeman.
- Kim, J. W., & Dang, C. V. (2005). Multifaceted roles of glycolytic enzymes. Trends in Biochemical Sciences, 30(3), 142-150.
- Vander Heiden, M. G., Cantley, L. C., & Thompson, C. B. (2009). Understanding the Warburg effect: the metabolic requirements of cell proliferation. Science, 324(5930), 1029-1033.
- Grace, R. F., et al. (2019). Mitapivat in Pyruvate Kinase Deficiency. New England Journal of Medicine, 381, 933-944.