Mekanisme Probiotik di Usus: Inhibisi Patogen, Penguatan Barrier, dan Modulasi Imun
Dalam ekologi gastrointestinal, probiotik dipahami sebagai mikroorganisme hidup yang, bila diberikan dalam jumlah memadai, dapat memberikan manfaat kesehatan pada inang. Di tingkat fisiologi usus, manfaat tersebut tidak muncul secara generik dari semua mikroba yang diberi label “probiotik”, melainkan dari interaksi biologis yang sangat bergantung pada galur, dosis, matriks penghantaran, mikrobiota dasar inang, dan kondisi mukosa usus. Karena itu, pembahasan mekanisme probiotik harus selalu dibaca dalam kerangka strain-specific activity, bukan sebagai sifat seragam dari seluruh genus seperti Lactobacillus, Bifidobacterium, atau probiotik secara umum.
Table Of Content
- Prinsip Dasar: Probiotik Bekerja dalam Konteks, Bukan dalam Ruang Hampa
- 1. Antagonisme Patogen: Dari Eksklusi Kompetitif hingga Interferensi Virulensi
- Sekresi Metabolit Antimikroba
- Eksklusi Kompetitif dan Persaingan Ruang Kolonisasi
- Interferensi terhadap Virulensi Patogen
- 2. Penguatan Sawar Intestinal: Menopang Integritas Epitel dan Lapisan Mukus
- Regulasi Tight Junction
- Stimulasi Produksi Mukus dan Fungsi Sel Goblet
- Perlindungan terhadap Cedera Epitel dan Stres Inflamasi
- 3. Modulasi Imun Mukosa: Dari Sensing Mikroba hingga Toleransi Imunologis
- Pengenalan MAMPs oleh Sistem Imun Mukosa
- Induksi Jalur Tolerogenik dan Sel T Regulator
- Peningkatan Produksi sIgA
- 4. Metabolit Mikroba sebagai Mediator Kunci
- 5. Hirarki Bukti: Mana yang Paling Mapan dan Mana yang Masih Berkembang?
- Matriks Integrasi Mekanisme Probiotik
- Keterbatasan Interpretasi Mekanisme Probiotik
- Kesimpulan
- Daftar Pustaka
- Terkait
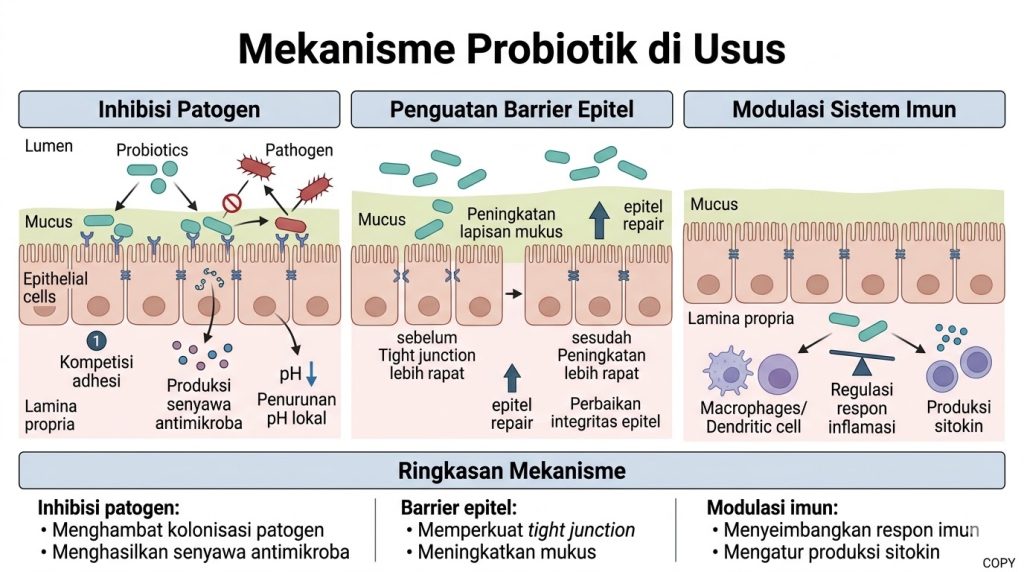
Pada saluran cerna, mekanisme kerja probiotik biasanya dipetakan ke dalam tiga sumbu besar. Pertama, probiotik dapat menekan kolonisasi dan virulensi patogen melalui antagonisme langsung maupun eksklusi kompetitif. Kedua, probiotik dapat mendukung integritas sawar mukosa dengan memengaruhi lapisan mukus, protein tight junction, dan ketahanan epitel terhadap stres inflamasi. Ketiga, probiotik dapat berinteraksi dengan sistem imun mukosa, terutama melalui komunikasi dengan sel dendritik, makrofag, sel B, dan sel T pada jaringan limfoid usus atau Gut-Associated Lymphoid Tissue (GALT).
Artikel ini membahas ketiga sumbu tersebut secara lebih disiplin, sambil membedakan mana mekanisme yang relatif mapan, mana yang sangat bergantung pada galur, dan mana yang masih terutama ditopang oleh bukti in vitro atau model hewan.
Prinsip Dasar: Probiotik Bekerja dalam Konteks, Bukan dalam Ruang Hampa
Sebelum masuk ke mekanisme spesifik, ada satu prinsip penting yang harus ditegaskan. Efek probiotik di usus tidak hanya ditentukan oleh identitas mikroba yang diberikan, tetapi juga oleh lanskap biologis tempat mikroba tersebut masuk. Lumen usus, lapisan mukus, permukaan epitel, dan lamina propria adalah kompartemen yang berbeda secara anatomi maupun fungsional. Sebuah galur dapat bertahan baik di lumen namun tidak melekat stabil pada mukus. Galur lain dapat menghasilkan metabolit yang kuat, tetapi kolonisasinya bersifat sementara. Karena itu, “keberhasilan” probiotik tidak dapat direduksi hanya menjadi pertanyaan apakah mikroba itu hidup atau tidak setelah dikonsumsi.
Selain itu, banyak mekanisme molekuler probiotik pertama kali dijelaskan pada model in vitro menggunakan sel epitel, sistem ko-kultur, atau model hewan. Bukti semacam ini sangat penting untuk menjelaskan mekanisme dasar, tetapi tidak selalu identik dengan efek klinis yang konsisten pada manusia. Oleh sebab itu, pembacaan mekanisme kerja probiotik yang baik harus memisahkan antara plausibilitas biologis dan kepastian luaran klinis.
1. Antagonisme Patogen: Dari Eksklusi Kompetitif hingga Interferensi Virulensi
Salah satu fungsi yang paling sering dibahas dalam studi probiotik adalah kemampuannya mengurangi beban atau agresivitas patogen enterik. Namun, mekanisme ini tidak hanya berarti “membunuh patogen”. Dalam banyak kasus, efek probiotik lebih tepat dipahami sebagai perubahan keseimbangan ekologi dan penurunan peluang patogen untuk menempel, tumbuh, atau mengekspresikan faktor virulensi secara optimal.
Sekresi Metabolit Antimikroba
Banyak bakteri asam laktat memproduksi asam organik seperti asam laktat dan asam asetat selama fermentasi karbohidrat. Akumulasi asam ini menurunkan pH lokal lumen atau mikro-nisah mukosa. Pada kondisi tertentu, bentuk asam yang tidak terdisosiasi dapat menembus membran patogen, lalu terdisosiasi dalam sitoplasma dan mengganggu homeostasis proton, proton motive force, serta keseimbangan energi sel. Konsekuensinya bukan selalu lisis instan, melainkan penurunan efisiensi metabolik, hambatan pertumbuhan, dan berkurangnya kemampuan patogen mempertahankan virulensi dalam lingkungan yang kompetitif.
Selain asam organik, sebagian galur probiotik menghasilkan senyawa antimikroba seperti bakteriosin. Bakteriosin adalah peptida atau protein antimikroba yang dapat menargetkan mikroba lain melalui pembentukan pori membran, gangguan integritas dinding sel, atau interferensi pada proses esensial tertentu. Contohnya, nisin dan plantaricin sering dipakai sebagai ilustrasi bagaimana produk metabolik bakteri asam laktat dapat berfungsi sebagai antagonis mikroba lain. Walau demikian, penting dicatat bahwa kemampuan menghasilkan bakteriosin tidak dimiliki secara merata oleh semua galur probiotik, dan spektrum kerjanya juga berbeda-beda.
Eksklusi Kompetitif dan Persaingan Ruang Kolonisasi
Infeksi enterik sering diawali oleh adhesi patogen ke mukus atau permukaan enterosit. Karena itu, kolonisasi awal merupakan tahap kunci dalam patogenesis. Sejumlah galur probiotik mengekspresikan protein adhesin, polisakarida permukaan, atau komponen dinding sel yang meningkatkan kemampuan mereka berinteraksi dengan mukus dan reseptor epitel. Bila galur probiotik berhasil menempati ruang ekologis tersebut terlebih dahulu, akses patogen ke lokasi yang sama dapat berkurang. Fenomena ini dikenal sebagai eksklusi kompetitif.
Mekanisme ini tidak semata-mata bersifat fisik. Dalam lumen yang nutrisinya terbatas, probiotik juga dapat ikut bersaing memperebutkan sumber karbon, nitrogen, logam transisi, dan komponen lain yang diperlukan patogen untuk proliferasi. Efek akhirnya adalah penurunan kebugaran ekologis patogen, bukan selalu eliminasi totalnya.
Interferensi terhadap Virulensi Patogen
Dalam beberapa penelitian, probiotik atau metabolitnya juga dilaporkan mampu menekan ekspresi gen virulensi patogen. Termasuk mekanisme yang terkait dengan quorum sensing, adhesi, produksi toksin, dan invasi epitel. Hal ini menunjukkan bahwa probiotik tidak selalu perlu membunuh patogen secara langsung untuk mengurangi dampak biologisnya. Pada sebagian model, cukup dengan mengubah lanskap kimiawi atau komunikasi antarbakteri, patogen dapat kehilangan sebagian kapasitas infeksinya. Namun, bukti mekanistik rinci untuk jalur ini masih sangat bergantung pada galur dan model yang digunakan.
2. Penguatan Sawar Intestinal: Menopang Integritas Epitel dan Lapisan Mukus
Epitel usus adalah antarmuka kritis antara lumen yang padat mikroba dan jaringan inang yang harus tetap terlindungi. Bila sawar ini terganggu, permeabilitas meningkat, endotoksin dan komponen mikroba dapat menembus lebih dalam, dan inflamasi menjadi lebih mudah dipicu. Karena itu, banyak studi probiotik berfokus pada pertanyaan apakah mikroba tertentu dapat membantu mempertahankan atau memulihkan integritas sawar usus.
Regulasi Tight Junction
Tight junction adalah kompleks protein yang menghubungkan sel epitel satu sama lain di sisi apikal dan mengontrol jalur paraseluler. Protein kunci dalam kompleks ini antara lain claudin, occludin, dan protein adaptor intraseluler seperti ZO-1 dan ZO-2. Sejumlah galur probiotik telah ditunjukkan mampu meningkatkan ekspresi atau redistribusi protein-protein ini, terutama pada model epitel yang mengalami stres inflamasi, paparan patogen, atau gangguan barrier.
Secara mekanistik, sinyal dari probiotik dapat diteruskan melalui berbagai jalur intraseluler, termasuk MAPK, PKC, AMPK, dan jalur-jalur lain yang bergantung pada tipe sel dan konteks stres. Aktivasi ini kemudian dapat mengubah transkripsi gen, stabilitas protein, atau lokalisasi kompleks tight junction di membran apikal. Yang penting, tidak semua laporan menunjukkan jalur yang sama, sehingga lebih akurat mengatakan bahwa probiotik tertentu dapat mendukung perakitan dan stabilitas tight junction, bukan bahwa semua probiotik bekerja melalui satu jalur tunggal yang seragam.
Stimulasi Produksi Mukus dan Fungsi Sel Goblet
Di atas permukaan epitel usus terdapat lapisan mukus yang kaya glikoprotein musin. Lapisan ini bukan sekadar pelapis pasif, tetapi komponen aktif dari sistem pertahanan mukosa. Mukus membatasi kontak langsung antara mikroba dan epitel, menjebak partikel, dan menjadi substrat ekologis bagi mikroba tertentu. Sejumlah studi menunjukkan bahwa probiotik tertentu dapat meningkatkan ekspresi gen musin seperti MUC2 dan memengaruhi aktivitas sel goblet. Hasilnya dapat berupa lapisan mukus yang lebih stabil atau peningkatan ketahanan terhadap kolonisasi patogen.
Namun, seperti halnya efek pada tight junction, dampak ini juga bersifat galur-spesifik. Tidak semua probiotik memberi efek yang sama pada ekspresi musin, dan tidak semua perubahan molekuler berujung pada luaran klinis yang identik.
Perlindungan terhadap Cedera Epitel dan Stres Inflamasi
Selain memengaruhi struktur sawar, probiotik dapat berkontribusi pada ketahanan epitel terhadap kerusakan oksidatif dan inflamasi. Efek ini dapat dimediasi oleh metabolit mikroba, interaksi dengan reseptor epitel, atau reduksi beban patogen. Dalam model eksperimental, hasilnya sering terlihat sebagai penurunan permeabilitas, penurunan translokasi molekul penanda, dan perbaikan morfologi jaringan. Tetapi sekali lagi, bagian pentingnya adalah bahwa data semacam ini sangat sering bergantung pada kondisi model dan tidak selalu bisa langsung ditranslasikan menjadi klaim terapeutik luas pada manusia.
3. Modulasi Imun Mukosa: Dari Sensing Mikroba hingga Toleransi Imunologis
Interaksi antara probiotik dan sistem imun mukosa adalah salah satu bidang yang paling kompleks. Komponen permukaan probiotik, fragmen dinding sel, DNA bakteri, serta metabolitnya dapat dikenali oleh sel imun atau sel epitel melalui pattern recognition receptors (PRRs) seperti Toll-like receptors (TLRs) dan NOD-like receptors. Interaksi ini tidak selalu menghasilkan aktivasi inflamasi. Dalam banyak konteks, sinyal justru mengarah pada pengaturan ulang respons imun menuju keadaan yang lebih tolerogenik atau lebih seimbang.
Pengenalan MAMPs oleh Sistem Imun Mukosa
Komponen seperti peptidoglikan, lipoteichoic acid, eksopolisakarida, dan DNA bakteri yang kaya motif CpG dapat bertindak sebagai microbe-associated molecular patterns (MAMPs). Sel dendritik dan makrofag di mukosa usus mengenali komponen ini melalui PRRs. Hasil pengenalan tersebut sangat bergantung pada tipe reseptor, intensitas sinyal, dan konteks lingkungan sitokin yang sudah ada. Karena itu, hubungan antara probiotik dan TLR2 atau TLR4 tidak sebaiknya dipahami secara linier atau tunggal. Sinyal dari reseptor yang sama dapat menghasilkan outcome yang berbeda bila konteks biologisnya berubah.
Induksi Jalur Tolerogenik dan Sel T Regulator
Salah satu outcome imunologis yang paling sering dibahas adalah peningkatan diferensiasi atau aktivitas regulatory T cells (Treg). Dalam berbagai model, probiotik tertentu mendorong sel dendritik menghasilkan sitokin seperti IL-10 dan TGF-β, yang kemudian mendukung pembentukan lingkungan imun yang lebih tolerogenik. Treg penting karena membantu menahan respons inflamasi berlebihan dan mempertahankan toleransi terhadap antigen makanan, mikrobiota komensal, dan rangsangan mukosa yang terus-menerus.
Pada titik ini, penting untuk sangat hati-hati. Tidak semua probiotik meningkatkan Treg dengan cara yang sama, dan tidak semua konteks inflamasi mendapat manfaat yang identik dari modulasi tersebut. Namun secara umum, kerangka biologis bahwa probiotik tertentu dapat menggeser respons imun ke arah regulasi yang lebih seimbang adalah salah satu bagian paling kuat dari literatur mekanistik probiotik.
Peningkatan Produksi sIgA
Sawar imun mukosa tidak lengkap tanpa antibodi secretory IgA (sIgA). Antibodi ini disekresikan ke lumen dan berfungsi mengikat mikroba maupun toksin, sehingga membantu menetralisasi patogen tanpa harus memicu inflamasi destruktif yang besar. Sejumlah probiotik dilaporkan dapat meningkatkan respons IgA mukosa, baik secara langsung melalui interaksi dengan Peyer’s patches maupun secara tidak langsung melalui modulasi lingkungan imun lokal. Efek ini sangat penting karena sIgA adalah salah satu alat utama tubuh untuk menjaga koeksistensi antara pertahanan dan toleransi di usus.
4. Metabolit Mikroba sebagai Mediator Kunci
Pembahasan probiotik modern tidak lengkap tanpa menyoroti peran metabolit. Dalam banyak kasus, yang berinteraksi dengan sel inang bukan hanya sel probiotik utuh, tetapi juga molekul yang dihasilkannya selama metabolisme. Asam organik, peptida bioaktif, eksopolisakarida, dan metabolit hasil interaksi silang dengan mikrobiota resident dapat bertindak sebagai mediator utama dari efek biologis probiotik.
Karena itu, ketika membahas “mekanisme probiotik”, kita sebenarnya membahas setidaknya tiga level agen biologis: sel hidup, komponen permukaan sel, dan produk metabolik. Ketiga level ini dapat berkontribusi secara bersamaan, dan proporsinya dapat berbeda pada tiap galur.
5. Hirarki Bukti: Mana yang Paling Mapan dan Mana yang Masih Berkembang?
Untuk menghindari pembacaan yang terlalu simplistik, mekanisme probiotik dapat dipetakan ke dalam hirarki bukti berikut:
- Relatif mapan secara biologis: produksi asam organik, antagonisme terhadap patogen, eksklusi kompetitif, pengaruh pada integritas barrier, dan keterlibatan modulasi imun mukosa.
- Sangat bergantung pada galur: produksi bakteriosin tertentu, pola adhesi spesifik, kekuatan induksi musin, pengaruh pada jalur sinyal tertentu, dan besar-kecilnya efek pada Treg atau sIgA.
- Sering masih bergantung pada model eksperimental: penjelasan detail jalur molekuler tertentu, interferensi quorum sensing spesifik, dan generalisasi luas dari hasil kultur sel atau hewan ke luaran klinis manusia.
Pembagian ini penting karena artikel ilmiah yang baik tidak hanya menjelaskan apa yang mungkin terjadi, tetapi juga seberapa kuat dasar buktinya.
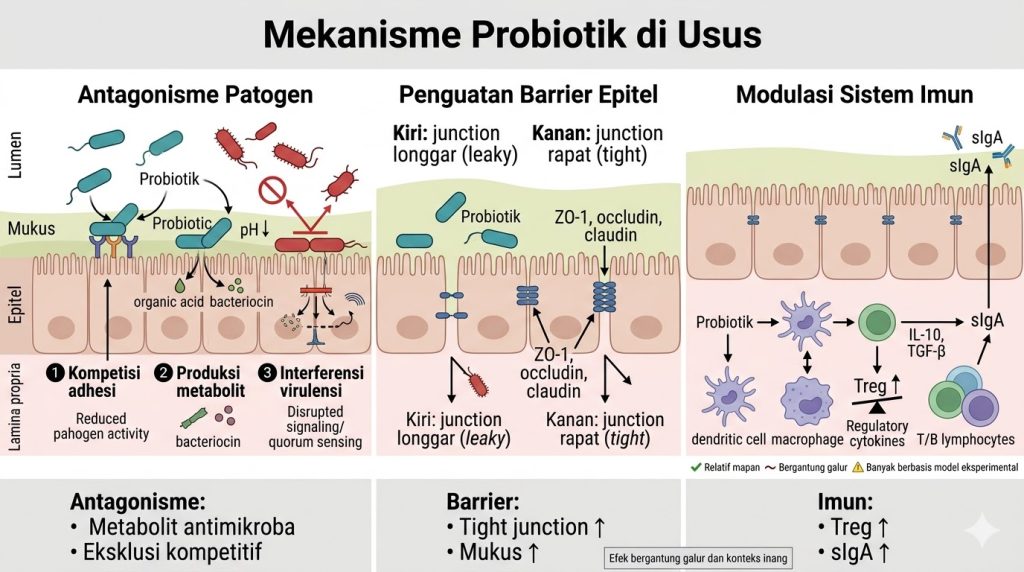
Matriks Integrasi Mekanisme Probiotik
| Mekanisme Aksi | Molekul / Mediator Efektor | Target Anatomi / Seluler | Luaran Biologis yang Diusulkan | Tingkat Nuansa Bukti |
|---|---|---|---|---|
| Antagonisme patogen | Asam organik, bakteriosin, metabolit antimikroba lain | Lumen usus, membran patogen, sistem virulensi patogen | Penurunan pertumbuhan, viabilitas, atau agresivitas patogen | Relatif mapan, tetapi besarnya efek sangat galur-dependent |
| Eksklusi kompetitif | Adhesin permukaan, eksopolisakarida, kompetisi nutrien | Mukus, reseptor epitel, ruang kolonisasi | Reduksi peluang adhesi dan kolonisasi patogen | Biologis kuat, tetapi sangat tergantung model dan strain |
| Penguatan tight junction | Sinyal seluler melalui MAPK/PKC/AMPK dan mediator lain | ZO-1, occludin, claudin, sitoskeleton apikal | Perbaikan integritas barrier dan penurunan permeabilitas | Kuat pada model eksperimental; translasi klinis bervariasi |
| Stimulasi mukus | Interaksi dengan sel goblet, regulasi gen musin | MUC2 dan lapisan mukus intestinal | Peningkatan perlindungan fisik terhadap kontak patogen-epitel | Didukung banyak model, tetapi tetap strain-dependent |
| Modulasi Treg | MAMPs, sitokin IL-10 dan TGF-β, aktivasi sel dendritik tolerogenik | Lamina propria, GALT, sel T naif | Lingkungan imun yang lebih terkontrol dan kurang proinflamasi | Konsep kuat, tetapi outcome tidak seragam antar strain |
| Peningkatan sIgA | Sinyal ke Peyer’s patches dan sel B mukosa | Lumen usus, sel plasma penghasil IgA | Netralisasi toksin dan aglutinasi patogen di lumen | Didukung secara biologis, tetapi magnitude klinis bervariasi |
Keterbatasan Interpretasi Mekanisme Probiotik
Pembacaan mekanisme probiotik harus menghindari tiga penyederhanaan yang terlalu umum. Pertama, tidak semua galur dalam satu spesies mempunyai profil kerja yang identik. Kedua, kolonisasi probiotik pada usus manusia sering bersifat sementara, sehingga keberadaan efek biologis tidak selalu bergantung pada kolonisasi permanen. Ketiga, mekanisme molekuler yang sangat rinci sering kali dihasilkan dari studi kultur sel atau hewan, sedangkan respons manusia nyata dipengaruhi diet, obat, penyakit dasar, komposisi mikrobiota awal, dan lama intervensi.
Karena itu, klaim mengenai probiotik yang baik harus selalu ditulis dengan bahasa yang terkalibrasi. Probiotik tertentu dapat mendukung barrier, dapat menggeser respons imun, atau dapat menurunkan kolonisasi patogen dalam kondisi tertentu. Bahasa seperti ini lebih akurat daripada menyatakan bahwa probiotik secara universal dan konsisten “menjamin” luaran tertentu pada semua individu.
Kesimpulan
Efek probiotik di saluran cerna merupakan hasil dari interaksi berlapis antara mikroba, epitel, mukus, patogen, metabolit, dan sistem imun mukosa. Secara umum, probiotik dapat bekerja melalui antagonisme terhadap patogen, eksklusi kompetitif pada permukaan mukosa, penguatan integritas sawar epitel, peningkatan fungsi mukus, dan modulasi respons imun menuju keadaan yang lebih seimbang. Namun, semua efek ini harus dibaca dalam kerangka strain-specificity dan context-dependence.
Bagi mahasiswa pascasarjana dan peneliti biosains, nilai utama dari studi probiotik bukan sekadar pada pertanyaan “apakah probiotik bermanfaat”, tetapi pada pertanyaan yang jauh lebih penting: galur mana, melalui mekanisme apa, pada kompartemen biologis yang mana, dan dengan tingkat bukti seperti apa. Di titik itulah analisis mekanistik probiotik benar-benar menjadi sains, bukan sekadar narasi promosi biologis.
Daftar Pustaka
- Bermudez-Brito, M., Plaza-Díaz, J., Muñoz-Quezada, S., Gómez-Llorente, C., & Gil, A. (2012). Probiotic mechanisms of action. Annals of Nutrition and Metabolism, 61(2), 160-174.
- Lebeer, S., Vanderleyden, J., & De Keersmaecker, S. C. J. (2008). Genes and molecules of lactobacilli supporting probiotic action. Microbiology and Molecular Biology Reviews, 72(4), 728-764.
- Plaza-Díaz, J., Ruiz-Ojeda, F. J., Gil-Campos, M., & Gil, A. (2019). Mechanisms of action of probiotics. Advances in Nutrition, 10(Suppl 1), S49-S66.
- Rose, E. C., Odle, J., & Blikslager, A. T. (2021). Probiotics, prebiotics and epithelial tight junctions. International Journal of Molecular Sciences, 22(13), 6729.
- Mazziotta, C., Tognon, M., Martini, F., Torreggiani, E., Rotondo, J. C. (2023). Probiotics mechanism of action on immune cells and beneficial effects on human health. Cells, 12(1), 184.
