Czapek’s Agar (CZA): Definisi, Biokimia, dan Standar Identifikasi Taksonomi Fungi
Czapek’s Agar (CZA) adalah media pertumbuhan mikrobiologis yang termasuk media sintetik terdefinisi (defined synthetic medium). Berbeda dari media alami atau kompleks yang memakai bahan biologis mentah, seperti ekstrak kentang pada Potato Dextrose Agar (PDA) atau pepton pada Sabouraud Dextrose Agar (SDA), komposisi kimia CZA ditetapkan secara presisi hingga tingkat molekuler.
Table Of Content
- Perbedaan Kunci dengan Media Fungi Lain (PDA/SDA)
- Komposisi dan Fungsi Biokimia
- Prinsip Kerja: Seleksi Nutrisi
- Konsep: Asimilasi Nitrogen Inorganik
- Prosedur Pembuatan
- Interpretasi Hasil dan Aplikasi Taksonomi
- 1. Karakteristik Koloni (Makroskopis)
- 2. Studi Morfologi (Mikroskopis)
- Daftar Pustaka
- Terkait
CZA diformulasikan untuk isolasi dan kultivasi fungi saprofit, bakteri tanah, serta mikroorganisme lain yang mampu memanfaatkan nitrogen anorganik sebagai sumber nitrogen.
Perbedaan Kunci dengan Media Fungi Lain (PDA/SDA)
Perbedaan paling mendasar antara Czapek’s Agar (CZA) dan media jamur standar lainnya terletak pada sumber nitrogennya. Media umum seperti PDA atau SDA menyediakan nitrogen dalam bentuk organik kompleks, misalnya asam amino dan peptida yang berasal dari pepton. Sebaliknya, CZA menggunakan natrium nitrat (NaNO₃) sebagai satu-satunya sumber nitrogen.
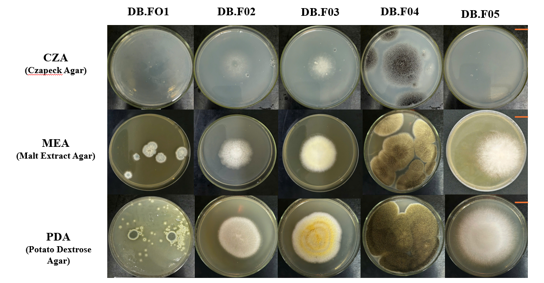
Konsekuensinya, CZA menciptakan tekanan selektif yang kuat karena hanya mikroorganisme dengan sistem enzim spesifik, terutama nitrat reduktase, yang mampu memanfaatkan nitrat sebagai sumber nitrogen dan tumbuh stabil pada media ini. Kondisi ini membuat CZA banyak digunakan untuk riset taksonomi kapang, khususnya genus Aspergillus dan Penicillium, karena media ini mendorong pembentukan karakter morfologi dan pigmen yang lebih konsisten. Pada media yang terlalu kaya nutrisi, karakter tersebut sering kurang tegas atau tidak stabil sehingga lebih sulit dipakai untuk pembeda taksonomi.
Komposisi dan Fungsi Biokimia
Formulasi CZA dirancang untuk menyediakan nutrisi esensial dalam bentuk garam mineral murni. Berikut adalah komposisi standar per liter akuades (pH akhir 7,3 ± 0,2 pada 25°C):
| Komposisi | Jumlah (g/L) | Fungsi Biokimia |
|---|---|---|
| Sukrosa (Saccharose) | 30,0 g | Sumber karbon utama untuk energi dan biosintesis sel. Konsentrasi tinggi mendukung tekanan osmotik yang disukai kapang. |
| Natrium Nitrat ($NaNO_3$) | 3,0 g | Sumber nitrogen inorganik tunggal. Menyeleksi organisme yang mampu mengasimilasi nitrat. |
| Dipotassium Phosphate ($K_2HPO_4$) | 1,0 g | Sistem buffer untuk menjaga stabilitas pH media dan sumber fosfor. |
| Magnesium Sulfat ($MgSO_4$) | 0,5 g | Sumber kation $Mg^{2+}$ yang berfungsi sebagai kofaktor enzim metabolik. |
| Kalium Klorida ($KCl$) | 0,5 g | Sumber ion esensial untuk keseimbangan osmotik dan fungsi seluler. |
| Ferrous Sulfate ($FeSO_4$) | 0,01 g | Sumber zat besi (trace element), kofaktor penting untuk produksi pigmen dan enzim sitokrom. |
| Agar | 15,0 g | Agen pemadat (solidifying agent). |
Prinsip Kerja: Seleksi Nutrisi
Mekanisme kerja CZA didasarkan pada kemampuan biosintesis mikroorganisme. Agar dapat tumbuh di media ini, fungi harus melakukan pekerjaan metabolik ekstra yang tidak diperlukan di media kaya nutrisi.
Konsep: Asimilasi Nitrogen Inorganik
Secara sederhana, PDA dapat dianalogikan sebagai “makanan siap saji” karena sumber nitrogen organik sudah tersedia dan mudah dimanfaatkan. Sebaliknya, CZA lebih menyerupai “bahan mentah” karena hanya menyediakan nitrat sebagai sumber nitrogen. Agar dapat memakainya, fungi harus memiliki “alat” berupa enzim nitrat reduktase untuk mereduksi nitrat (NO₃⁻) menjadi nitrit (NO₂⁻), lalu menjadi amonia (NH₄⁺) sebelum nitrogen tersebut dapat digunakan dalam sintesis asam amino dan protein seluler.
Karena rangkaian reduksi ini membutuhkan energi tambahan, pertumbuhan koloni pada CZA umumnya lebih lambat dan tidak selebat pada PDA. Namun, kondisi nutrisi yang lebih terbatas sering menghasilkan pembentukan struktur mikroskopis yang lebih jelas dan khas, termasuk konidia dan spora. Akibatnya, CZA lebih membantu untuk pengamatan morfologi dan identifikasi dibanding media yang terlalu kaya nutrisi.
Prosedur Pembuatan
Pembuatan CZA memerlukan ketelitian, terutama dalam penanganan larutan garam mineral untuk mencegah presipitasi (pengendapan) yang dapat mengganggu kejernihan media.
- Penimbangan: Timbang seluruh bahan kimia sesuai formulasi. Penggunaan timbangan analitik sangat disarankan untuk komponen mikro seperti Ferrous Sulfate.
- Pelarutan Bertahap: Larutkan bahan-bahan dalam sebagian besar akuades (sekitar 900 mL).
Catatan Teknis: Sebaiknya larutkan Ferrous Sulfate secara terpisah dalam volume kecil air, lalu tambahkan terakhir ke dalam campuran utama. Hal ini mencegah interaksi kimia dini yang menyebabkan endapan keruh sebelum sterilisasi. - Pemanasan: Panaskan campuran hingga mendidih (boiling) di atas hot plate sambil diaduk untuk melarutkan agar sepenuhnya.
- Sterilisasi: Sterilkan menggunakan autoklaf pada suhu 121°C, tekanan 15 psi, selama 15 menit.
- Penuangan: Dinginkan media hingga suhu 45-50°C, lalu tuang ke dalam cawan petri steril secara aseptis.
Interpretasi Hasil dan Aplikasi Taksonomi
Dalam mikologi diagnostik, CZA bukan sekadar media pertumbuhan, melainkan alat identifikasi. Pengamatan dilakukan setelah inkubasi pada suhu 25-30°C selama 5-7 hari (atau lebih, tergantung spesies).
1. Karakteristik Koloni (Makroskopis)
Ahli taksonomi menggunakan CZA untuk mendeskripsikan warna koloni yang “sebenarnya”. Kandungan nutrisi yang terbatas memaksa fungi memproduksi metabolit sekunder (pigmen) yang spesifik.
- Permukaan Koloni: Perhatikan tekstur (beludru, kapas, berbutir) dan warna spora. Contoh: Aspergillus flavus akan menunjukkan warna hijau kekuningan yang khas pada CZA.
- Reverse Koloni: Warna bagian bawah koloni (dilihat dari balik cawan petri) sangat krusial. Beberapa spesies Penicillium memproduksi pigmen merah atau kuning yang berdifusi ke dalam agar CZA, sebuah ciri yang mungkin tidak muncul di media lain.
2. Studi Morfologi (Mikroskopis)
Pada CZA, pertumbuhan vegetatif berupa hifa umumnya tidak terlalu dominan. Kondisi ini mendorong pembentukan struktur reproduksi, seperti konidiofor, vesikel, dan fialid, yang tampak lebih jelas saat diamati di bawah mikroskop. Kejelasan struktur tersebut mempermudah identifikasi spesies menggunakan kunci determinasi standar.
Daftar Pustaka
- Atlas, R. M. (2010). Handbook of Microbiological Media. 4th Edition. CRC Press.
- Pitt, J. I., & Hocking, A. D. (2009). Fungi and Food Spoilage. 3rd Edition. Springer.
- Samson, R. A., et al. (2014). Food and Indoor Fungi. CBS-KNAW Fungal Biodiversity Centre.
- Nguyen, V. C., Nguyen, T. K. T., Nguyen, T. H. T., & Ngo, C. C. (2025). Biological characteristics of some filamentous fungal strains isolated from rubber surface at the Dam Bay Marine Climatic Testing Station, Nha Trang. Journal of Tropical Science and Engineering, 39, 107–122. https://doi.org/10.58334/vrtc.jtst.n39.727

