
Triple Sugar Iron Agar (TSI): Prinsip Dasar, Prosedur, dan Interpretasi Hasil
Medium Triple Sugar Iron Agar (TSIA) adalah media diferensial yang digunakan secara luas dalam laboratorium mikrobiologi untuk mengidentifikasi bakteri batang Gram-negatif, khususnya dari famili Enterobacteriaceae. Media ini diformulasikan secara khusus untuk membedakan mikroorganisme berdasarkan perbedaan kemampuan metabolik mereka, terutama dalam memfermentasi tiga jenis karbohidrat spesifik serta kemampuan memproduksi gas hidrogen sulfida.
Table Of Content
- Prinsip Kerja dan Reaksi Biokimia TSIA
- 1. Fermentasi Karbohidrat (Rasio 10:10:1)
- 2. Produksi Hidrogen Sulfida ($H_2S$)
- 3. Pembentukan Gas
- Komposisi Media
- Metodologi dan Prosedur Kerja
- Persiapan Media
- Teknik Inokulasi
- Interpretasi Hasil
- Keterbatasan Uji dan Kontrol Kualitas
- Kesimpulan
- Daftar Pustaka
- Terkait
Prinsip Kerja dan Reaksi Biokimia TSIA
Efektivitas diagnostik TSI Agar didasarkan pada interaksi antara metabolisme bakteri dengan indikator kimiawi dalam media. Indikator pH yang digunakan adalah Fenol Merah (Phenol Red), yang akan menunjukkan perubahan warna dari merah (pH > 7,4, kondisi basa) menjadi kuning (pH < 6,8, kondisi asam) seiring dengan pembentukan asam organik hasil fermentasi.
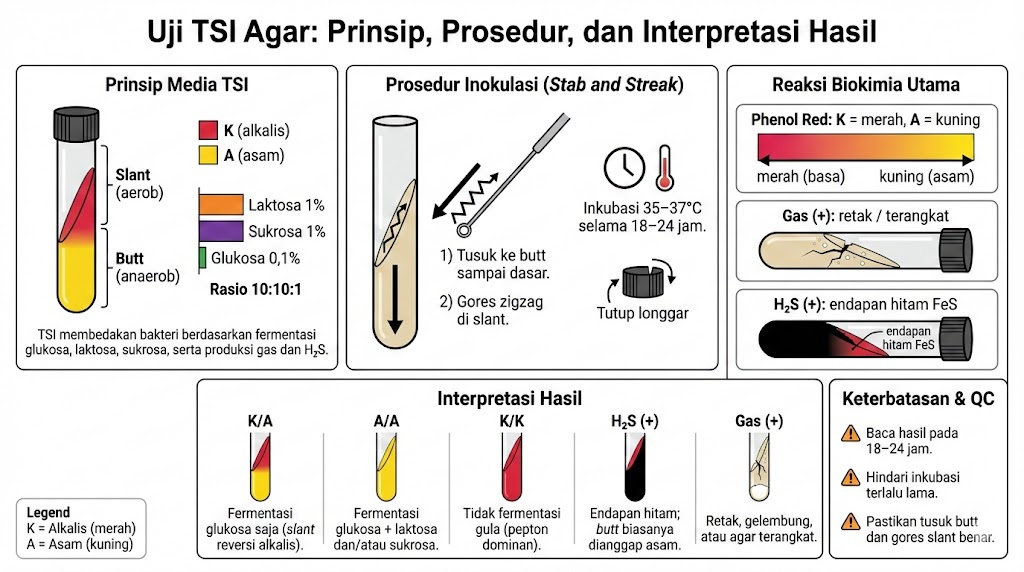
1. Fermentasi Karbohidrat (Rasio 10:10:1)
Karakteristik unik TSI terletak pada komposisi gulanya: Laktosa (1%), Sukrosa (1%), dan Glukosa (0,1%). Rasio konsentrasi ini krusial untuk membedakan pola fermentasi:
- Fermentasi Glukosa Saja: Karena konsentrasi glukosa sangat rendah, asam yang dihasilkan akan cepat teroksidasi di bagian permukaan miring (slant) yang bersifat aerob. Setelah glukosa habis (sekitar 12 jam), bakteri akan beralih memecah pepton (deaminasi oksidatif) yang menghasilkan amonia bersifat basa. Hal ini menyebabkan slant kembali berwarna merah (fenomena reversi alkalis), sementara bagian dasar (butt) yang anaerob tetap berwarna kuning karena akumulasi asam yang stabil.
- Fermentasi Laktosa dan/atau Sukrosa: Jika bakteri mampu memfermentasi laktosa atau sukrosa yang berkonsentrasi tinggi (10x lipat glukosa), produksi asam akan terus berlanjut secara masif hingga akhir masa inkubasi. Kapasitas penyangga (buffer) media akan terlampaui, sehingga kondisi asam bertahan di seluruh tabung (slant dan butt berwarna kuning).
2. Produksi Hidrogen Sulfida ($H_2S$)
Deteksi $H_2S$ dimungkinkan oleh adanya natrium tiosulfat sebagai sumber sulfur dan ferrous ammonium sulfate sebagai indikator. Pada suasana asam, bakteri yang memiliki enzim tiosulfat reduktase akan mereduksi tiosulfat menjadi gas $H_2S$. Gas ini bereaksi dengan ion besi ($Fe^{2+}$) membentuk endapan hitam besi sulfida ($FeS$) yang tidak larut, umumnya terlihat pada perbatasan antara butt dan slant.
3. Pembentukan Gas
Produksi gas ($CO_2$ dan $H_2$) sebagai produk sampingan fermentasi ditandai dengan adanya retakan pada media agar, terangkatnya media dari dasar tabung, atau munculnya gelembung udara yang terperangkap.
Komposisi Media
Berikut adalah komposisi standar TSI Agar per liter akuades (pH akhir 7,4 ± 0,2 pada suhu 25°C):
| Komposisi | Jumlah (g/L) | Fungsi |
|---|---|---|
| Digest Pankreatik Kasein | 10,0 g | Sumber nitrogen dan asam amino. |
| Digest Peptik Jaringan Hewan | 10,0 g | Sumber nitrogen tambahan. |
| Laktosa | 10,0 g | Karbohidrat diferensial (konsentrasi tinggi). |
| Sukrosa | 10,0 g | Karbohidrat diferensial (konsentrasi tinggi). |
| Glukosa (Dextrose) | 1,0 g | Karbohidrat fermentasi dasar (konsentrasi rendah). |
| Ferrous Ammonium Sulfate | 0,2 g | Indikator $H_2S$. |
| Natrium Klorida | 5,0 g | Keseimbangan osmotik. |
| Natrium Tiosulfat | 0,3 g | Sumber sulfur. |
| Fenol Merah | 0,025 g | Indikator pH. |
| Agar | 12,0 g | Agen pemadat. |
Metodologi dan Prosedur Kerja
Persiapan Media
- Larutkan serbuk media dalam akuades dan panaskan hingga mendidih (boiling) untuk melarutkan agar secara sempurna.
- Sterilisasi menggunakan autoklaf pada suhu 121°C dengan tekanan 15 psi selama 15 menit.
- Dinginkan tabung reaksi dalam posisi miring untuk membentuk bagian lereng (slant) sepanjang ±2,5 cm dan bagian dasar (butt) sedalam ±2,5 cm. Proporsi ini penting untuk menjaga keseimbangan kondisi aerob dan anaerob.
Teknik Inokulasi
- Gunakan jarum inokulasi (ose lurus/needle) steril.
- Ambil koloni bakteri murni (usia kultur 18-24 jam).
- Lakukan inokulasi dengan metode tusuk dan gores (stab and streak): Tusukkan jarum tegak lurus hingga mencapai dasar tabung, kemudian saat menarik jarum, goreskan sisa inokulum secara zigzag pada permukaan lereng.
- Tutup tabung tidak terlalu rapat (longgar) untuk memastikan pertukaran udara pada bagian lereng agar deaminasi oksidatif dapat terjadi.
- Inkubasi pada suhu 35-37°C selama 18-24 jam.
Interpretasi Hasil
Pembacaan hasil dilakukan dengan mengamati perubahan warna pada bagian lereng (aerob) dan dasar (anaerob). Dalam terminologi laboratorium, hasil dinyatakan sebagai Asam (A) untuk warna kuning dan Alkalis (K) untuk warna merah.
| Lereng (Slant) | Dasar (Butt) | Interpretasi Metabolisme | Simbol | Contoh Bakteri |
|---|---|---|---|---|
| Merah (Alkalis) | Kuning (Asam) | Fermentasi glukosa saja. Pepton dikatabolisme di lereng. | K/A | Shigella flexneri, Salmonella Typhi |
| Kuning (Asam) | Kuning (Asam) | Fermentasi glukosa serta laktosa dan/atau sukrosa. | A/A | Escherichia coli, Klebsiella pneumoniae |
| Merah (Alkalis) | Merah (Alkalis) | Tidak ada fermentasi gula. Pepton dikatabolisme aerob dan anaerob. | K/K | Pseudomonas aeruginosa |
| Hitam | Kuning/Merah | Produksi $H_2S$. (Warna dasar tertutup endapan biasanya dianggap asam). | $H_2S$ (+) | Proteus mirabilis, Salmonella sp. |
| Pecah/Terangkat | – | Produksi Gas ($CO_2$ dan $H_2$). | Gas (+) | Enterobacter aerogenes |
Keterbatasan Uji dan Kontrol Kualitas
Terdapat beberapa batasan teknis yang perlu diperhatikan agar tidak terjadi kesalahan interpretasi (misleading results):
- Waktu Inkubasi: Pembacaan hasil sebelum 18 jam dapat menyebabkan hasil false-acid pada lereng karena reversi alkalis belum terjadi. Sebaliknya, inkubasi lebih dari 24 jam dapat menyebabkan keseluruhan tabung menjadi merah karena habisnya seluruh sumber karbohidrat dan penggunaan pepton secara total.
- Perbedaan dengan KIA: TSI Agar sering disamakan dengan Kligler Iron Agar (KIA). Perbedaan mendasar terletak pada penambahan Sukrosa pada TSI. Hal ini memungkinkan TSI untuk mendiferensiasi bakteri fermentor sukrosa (seperti Proteus vulgaris dan Yersinia enterocolitica) yang akan memberikan hasil A/A pada TSI namun K/A pada KIA.
Kesimpulan
Uji TSI Agar merupakan metode yang efisien dan informatif untuk karakterisasi awal bakteri Gram-negatif. Dengan memahami prinsip biokimia di balik setiap perubahan warna dan endapan, praktikan dapat mengidentifikasi genus bakteri secara presumtif sebelum dilanjutkan dengan uji serologi atau molekuler lebih lanjut.
Daftar Pustaka
- Cappuccino, J. G., & Welsh, C. (2018). Microbiology: A Laboratory Manual. 11th Edition. Pearson Education.
- Leboffe, M. J., & Pierce, B. E. (2011). A Photographic Atlas for the Microbiology Laboratory. 4th Edition. Morton Publishing Company.
- Mahon, C. R., & Lehman, D. C. (2019). Textbook of Diagnostic Microbiology. 6th Edition. Elsevier Health Sciences.
